生物与食品工程学院生物制药与载体材料工程研究团队(生物工程学科)成功构建了基于巨噬细胞的主动肿瘤靶向药物递送系统用于肿瘤的靶向治疗,实现了纳米药物载体在肿瘤部位的高效靶向递送。相关研究成果以“Pluronic-based nanoparticles for delivery of doxorubicin to the tumor microenvironment by binding to macrophages”为题,发表在《ACS Nano》(中科院一区TOP,IF:17.1)。安徽工程大学为该论文第一通讯作者单位,生物与食品工程学院2024届研究生胡成锐为论文第一作者。
传统化疗作为目前治疗肿瘤的主要手段之一,存在毒副作用强,易复发等问题。基于纳米颗粒的载药系统可有效提高药物在肿瘤部位的蓄积以减轻毒副作用,已成为提高肿瘤治疗效果的一种有效策略。然而,目前已报道的纳米颗粒在临床试验中并不能转化为更好的疗效,因其在血液循环中会迅速被免疫清除,缺乏特异性的靶向肿瘤,而且在肿瘤组织中的扩散也受到限制。朱龙宝教授团队创新性地利用巨噬细胞等内源性细胞的肿瘤归巢特性,开发出新型的主动靶向给药系统,解决肿瘤治疗中传统载药输送系统存在的问题。
团队利用巨噬细胞表面的CCR2/MCP-1信号轴为基础构建递送平台。首先通过固相合成成功获得MCP-1多肽,而后通过酯化反应成功将普朗尼克F127(PF127)末端羟基改性成为羧基,然后利用EDC/NHS反应成功将多肽MCP-1与PF127连接制备出纳米载体MPM,MPF自组装过程中包载肿瘤化疗药物阿霉素(DOX),初步构建靶向纳米药物载体(DMPM)。DMPM在信号轴CCR2/MCP-1的介导下能与巨噬细胞RAW264.7自发结合成DMPM-RAW264.7,然后巨噬细胞利用归巢特性引导DMPM在肿瘤内部富集,并实现药物的定向释放,显示出较高的肿瘤治疗效果。
此研究开发出新的基于巨噬细胞的纳米药物递送平台,该平台实现了DMPM的高效输送并在一定程度上提升了机体的肿瘤免疫性,构建的CCR2/MCP-1信号轴介导的巨噬细胞主动靶向药物输送系统可以用于药物的输送及治疗,为肿瘤治疗提供了新的思路与方式,具有良好的应用前景。
原文链接:https://pubs.acs.org/doi/full/10.1021/acsnano.4c01120
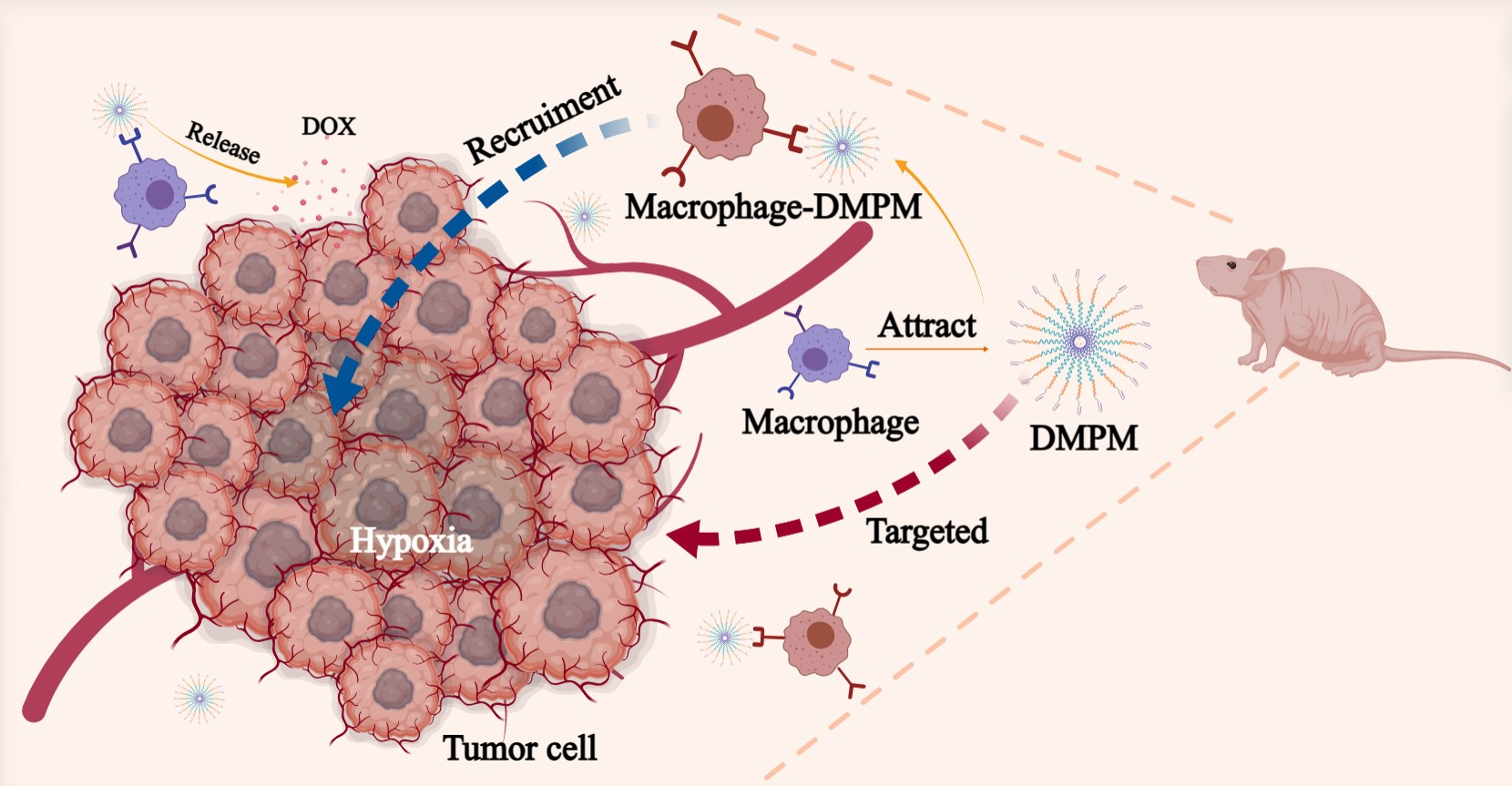
(文:朱龙宝、张伟伟;图:胡成瑞;审核:葛飞、王宗乾)

